人胰岛样类器官的制备方法_再造胰岛能否实现
目前全球有约4.6亿糖尿病患者,每年有420万人死于糖尿病,我国有近1.3亿糖尿病患者。在 1 型糖尿病中,胰岛β细胞遭到机体免疫系统无情地破坏,部分或完全失去了分泌胰岛素的功能,造成体内胰岛素绝对缺乏,引起了血糖水平持续升高,于是糖尿病出现了。胰岛移植虽可以改善患者的胰岛素不足问题,但是供源不足,临床上无法大规模开展。
近年来,蓬勃发展的干细胞技术解决了一部分细胞来源问题,但也存在局限性——胰岛β细胞的转化率低、稳定性差等。因而建立一个稳定高效的胰岛β细胞制备方案很重要。
本文综述了细胞起源、生物材料和用于制造人类胰岛类器官的先进技术的最新进展,并讨论了它们的优点、缺点和未来的挑战。作者望这篇综述能为构建人类胰岛类器官提供一个跨学科的视角,并为组织工程和再生医学提供见解。
1、胰岛β细胞是目标
人类胰岛
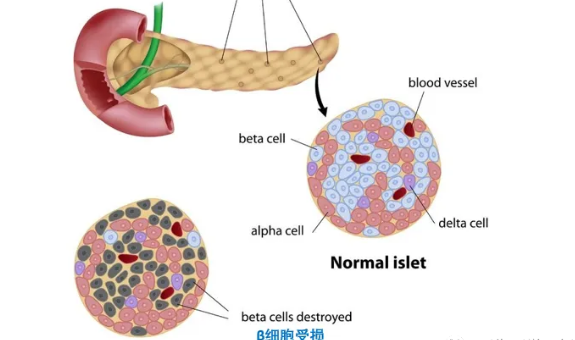
人体的胰岛素来源胰岛,胰岛是许多大小不等和形状不定的细胞团,散布在胰腺的各处。胰岛中的细胞主要由α细胞,β细胞,δ细胞和pp细胞组成。
1型糖尿病是由胰岛β细胞受损,导致胰岛素分泌绝对不足造成的。
1型糖尿病发病机制
胰岛素是机体内唯一可以降低血糖的激素,由胰岛β细胞分泌而来。针对 1 型糖尿病,想要拯救分泌不足的胰岛素,生产源源不断的可分泌胰岛素的 β细胞是目标。
类器官
类器官(Organoid),最早定义是通过细胞分离和重聚来模拟器官发生。自2009年,荷兰科学家Clevers团队开发小肠类器官以来,类器官的定义变成了由器官特异性细胞组成的三维(3D)结构,其来源于多能干细胞(PSC)或成人干/祖细胞。
类器官organoid被描述为“体外微型器官”或某种程度上的“人造器官”,可模拟体内器官景观,展示体内发现的一系列细胞类型,并展示器官功能的某些方面。Organoid技术已经成为一种工具,可弥合细胞和组织/器官水平的生物模型之间的差距,在保留某些生理功能的同时,更真实地描述体内组织的空间组织以及细胞和细胞外环境之间的相互作用。
在过去的十年中,胰岛类器官作为一种很有希望的糖尿病模型引起了越来越多的关注,它可以揭示胰岛相关疾病的机制,并且是一个测试药物效力和毒性的良好平台。例如,胰岛类器官可以填补我们有关早期(8周妊娠)和晚期妊娠人类胰腺组织(妊娠22周)的人类胰腺发育知识的空白,有望成为糖尿病治疗中移植的新胰岛资源。
2、制造人类胰岛类器官的细胞
构建胰岛类器官,需要胰腺内分泌细胞。适合构建胰岛类器官的细胞类型,包括:1)人类多能干细胞来源的胰岛细胞;2)通过去分化和再分化在成人胰岛中富集的胰腺内分泌细胞;3)非胰岛谱系细胞(如导管、腺泡细胞和肝细胞)。
不同方案制备胰岛类器官,在结构和功能上存在显著差异。同时,辅助细胞(包括内皮细胞和间充质细胞)在胰岛类器官形成过程中有促进作用。
能起支持作用。胰岛有丰富的血管供应,为人类胰岛提供充足的氧气、营养供应、微调血糖传感和调节。内皮细胞可以产生多种因子,如结缔组织生长因子、骨形态发生蛋白2(BMP-2)和BMP-4,可增加人ESC衍生的胰腺祖细胞贴壁培养中胰岛素的表达,并介导胰岛特异性成熟。例如,HUVEC或内皮细胞已与人类胰腺祖细胞或内分泌βH1β细胞混合,以促进胰岛类器官的自我聚集、成熟和血管化[35、39、57]。除了外源性添加内皮细胞外,内皮生长因子还可以诱导人胰岛类器官的血管生成。
血管生成素-2已被证明在胰岛类器官内诱导VE钙粘蛋白+内皮细胞和NG2+周细胞的广泛传播。此外,血管生成素-2可以部分补充内皮细胞对β细胞的体内旁分泌刺激,通过促进F-肌动蛋白重塑和调节钙离子内流动力学,使人类胰岛类器官具有天然的葡萄糖刺激胰岛素分泌水平。
MSC也参与胰岛样类器官的构建,包括自组织、血管网络的构成和旁分泌功能:
(a)间充质细胞触发自凝,这种由肌动球蛋白细胞骨架轴产生的牵引力导致细胞群的定向和剧烈运动。
(b) 在肌内人胰岛移植模型中,除了触发自凝聚外,间充质细胞还支持内皮细胞相互作用:人胰岛内皮细胞从移植中心迁移到周围组织,与受体内皮细胞形成嵌合血管;
(c) 据报道来自骨髓的大鼠间充质细胞通过释放HGF和TGFβ等营养因子,在水凝胶环境中支持包裹的小鼠胰岛,葡萄糖激发后胰岛素分泌增加。
3、制造人类胰岛类器官的材料
人胰岛类器官中的生物材料可以为细胞提供3D结构的支持、细胞外环境(ECM)的模拟以及在移植后的隔离保护。
乎自然的微环境,但有几个限制妨碍了它们的临床应用:
a)获得dECM凝胶的过程,包括脱细胞、提取和纯化,既耗时又昂贵;
b)原材料资源,尤其是生物质资源的批次间可变性;
c)几乎不可能控制生物物理性质和生化成分;
d)这些凝胶来自可能遭受细胞相容性和病原体传播的生物体。
用于人类胰岛类器官构建的合成基质材料
用于药物治疗的合成基质材料通常具有生物相容性和无毒性,具有可控性、再现性、降解性和良好的机械性能等优良特性。
常见的合成聚合物包括聚乙二醇(PEG)及其衍生物、聚乳酸(PLA)、聚乳酸-乙醇酸(PLGA)、聚乙烯醇(PVA)、聚己内酯(PCL)。根据具体应用,合成基质可以定制为不同的特性,例如,提供ECM特性以增强体外细胞间的相互作用,并模拟天然胰岛的硬度,这使得合成基质成为一种有前途的基质材料。
PCL是一种具有高机械稳定性的生物相容性和生物可降解聚酯,通过将PCL与价格合理、热稳定性高、亲水性强的PVA混合,可以改善其较差的细胞亲和性。基于PEG的基质也是一种多功能工具,用于模拟细胞微环境,并为人类胰岛类器官提供平台。
3D培养为类胰岛提供一个更真实的环境和结构组织,类似于天然人类胰岛。构建的标准方法包括传统的自聚集法、改良的自聚集法和水凝胶包埋法。还将讨论3D生物打印、脱细胞器官支架和芯片上器官等新出现的方法(图3)。
可以形成胰岛细胞的三维结构,提供模拟胰岛自然生态位的细胞-细胞外基质相互作用,而且有助于其长期存活。为了维持移植后胰岛在体内的可持续性,“胰岛包裹”可能是一个很好的策略。包封方法就像一个胶囊,由被基质材料包围的胰岛组成。
Stock及其同事用聚乙二醇-马来酰亚胺(PEG-MAL)与二硫代PEG(SH-PEG-SH)交联制成的保形涂层,并辅以PepGel肽和PEG低聚乙硫醚(PEG-OES)纳米纤维,将源自人类干细胞的类胰岛有机物包裹起来。在这项研究中,胰岛样类器官在体外与未包封的胰岛保持相当的胰岛素分泌曲线和刺激指数长达7天,甚至可以防止在海藻酸钠和聚乙二醇-海藻酸钠较大微囊中包封的胰岛中可见的中央坏死。此外,将胰岛类器官移植到糖尿病小鼠体内,使糖尿病得以长期逆转,并在没有免疫抑制的情况下维持正常血糖80天以上。
5、挑战和展望
目前人胰岛类器官的发展道路上还存在着三大挑战:类器官中胰岛细胞类型、比例以及空间位置错乱;类器官的批次、个体之间的巨大差异性;受到免疫排斥、缺氧等因素影响,移植后的胰岛类器官存活率低。
胰岛类器官可以促进人类胰岛的研究,尤其是在人类胰岛发育、糖尿病疾病模型和胰岛移植领域。自从埃德蒙顿方案首次获得成功以来,胰岛并不是移植的唯一来源。近年来,基于干细胞的糖尿病临床试验已经被提出并实施。2014年,ViaCyte提交了人类ESC源性胰腺祖细胞移植治疗T1D的首次试验(NCT02239354)。2021年1月,SEMMA启动了一项HESC来源的β细胞治疗T1D的临床试验。
蓬勃发展的人类胰岛再生无疑将使再生医学更接近糖尿病患者,并有望补充遗体胰岛的临床移植需求。
全生命周期基因健康管理致力于先进生物医学技术研发,全力推动科研成果临床转化与应用,是一家集生命科学研究,细胞资源存储,细胞治疗,细胞药品、细胞衍生品、保健品及化妆品的研发、生产、销售于一体的健康服务机构。
参考资料:
我们尊重原创。部分文字美图素材来源于网络,版权属于原作者。文章推送时因种种原因未能与原作者联系上,若涉及到版权问题,敬请原作者联系我们,立即处理。
复合小分子肽主要成分:人参(五年以下人工种植)、牛骨髓肽、海洋鱼低聚肽、牡蛎肽、地龙蛋白肽、苦瓜肽、纳豆粉、菊粉

咨询微信:591574114
说明:本站分享的产品是食品,不是药物,不能代替药物和医院治疗疾病!
分享内容均转自互联网,仅做参考,如您有疾病,建议您去看医生!我们理念是平时要注重养生与营养!
温馨提示:为了您的健康,克制不良的生活习惯,戒烟、限酒,不吃各种油炸食品、方便面、烧烤肉类、少吃工厂的各种加工食品,多吃新鲜蔬菜、水果,适当增加粗粮,配合服用等,详情咨询客服!
特别声明:本文来源于网络,如有侵权我们深感歉意,请联系我们,定在第一时间删除!
本文归原创所有,如有转发请标明原创出处。
